选课中心NEW
7099人选课
SAT【0】元讲座
免费学
托福【0】元讲座
免费学
SAT模考网站HOT
39209人预约
托福备考练习HOT
39209人预约
SAT辅导课程NEW
免费报名
AP辅导课程NEW
立即报名
中学生托福课程NEW
立即报名
大学生托福课程NEW
立即报名
【定制】1v1
私人订制
【资料】考前冲刺
精

扫码添加助教
免费领取
备考资料大礼包

扫码关注公众号
SAT2考试中,化学部分也是很多同学会选择的考试科目。具体的这部分考试中,重点考察的化学公式以及知识点都有哪些呢?这里为大家进行统一的梳理,详细内容如下:
来源:上海新东方 赵鑫

limiting
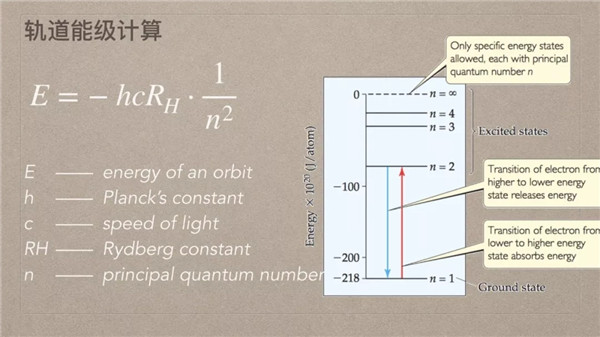
reagent在英文中叫限制反应物,在中文里叫过剩反应物,其实是同一概念的不同表达。计算也比较简单,化学反应方程式一定要配平,在反应物的系数下面,直接写下这个反应物给你提供的初始浓度,再去利用这个初始浓度的比值与系数之比进行判断,数值较小的那个比值,比如说x/a 上图主要就是辐射性,也是核反应,再具体一点就是核裂变。那我们重点讲这个辐射性的体现,一个叫α裂变,一个叫β裂变,α裂变出来的产物是两个质子和两个中子组成的氦原子核,也就是我们所谓的α粒子。β裂变,β负裂变,指的就是释放出电子的反应。 看上图的例子,比如说U238这个同位数,它可以去裂变,对外释放出两个质子、两个中子,之后它就会裂变成钍这个元素,再释放出α粒子,这是α-decay。比如说这个得到的钍,它也可以去发生一个β-decay,我们发现它的质子数由90变成了91,但是它的核子数还是234,那是因为β-decay是把中子转变成质子的反应,这样的话为了保持电量的平衡,你需要去释放一个负电的电子。所以,这两个反应学会配平就好。 下图是轨道的能级: 那它重点其实是解释氢原子光谱的不连续性,这个概念其实有点难懂,如果没有听过的同学,尽量尝试去听一下。 所有的原子,其实都是有很多很多级的轨道,比如说有第一层轨道,第二层轨道,那这个第一、第二,就是我们所说的principal quantum
number,叫做主量子数,指的是第几层的层数。电子处于不同的层级上、不同的轨道中,会具有不同的能量,这个能量的计算公式参照上图,但是不需要记录这么多,你只需要注意一下几个点: 1、电子轨道的能级都是负的。 2、它和主量子数的平方成反比。即如果它的N越大,负的就越多,能量也就越低。 在化学里面有一句话一定要注意,叫能量越低越稳定。所以,N=1是能量最低的轨道,被我们称之为基态。如果N=2,它的能量会更高一点,它负的更少,能量更高。那么,这个电子从N=1的轨道向N=2的轨道上面进发的话,被我们称之为激发态,因为它能量更高。比如说今天人比较多,我有一点人来疯,那我就激发了,我的能量会更高一点。所以电子也是这样的,N=1的基态跃迁到N=2的激发态的话,需要吸收能量,这个能量就可以用△E来表示。 刚才我们说到了,电子它吸收的能量,或者说释放的能量,比如说从激发态回到基态的过程当中,它就要释放能量。那么,这个释放的能量刚好就是两个轨道之间的能量之差,这其实也就在解释,为什么氢原子在激发过后,释放的光,它不是一个连续的光谱。 我们来看这个光子的能量。光子的能量是量子力学提出来的一个概念,ν是希腊字母,表示光子的频率,你也可以认为是某种光的频率。那么,h是Planck's
constant,顾名思义,为纪念普朗克的一个常量。在这里的话,由于电子从较高的轨道回到能量较低的轨道当中释放的能量,会以光的形式呈现,这个能量又是固定的,所以它释放出来光的颜色也是固定的。我们知道光的颜色和波长是有关的。 以上就为大家整理的“SAT2化学常用公式:limiting reagent”,更多精彩内容,请关注新东方在线SAT频道。 SAT水平能力测试【0元免费测试】


 资料下载
资料下载
【SAT】SAT官方指南题目合集10套
发布时间:2024-04-15添加新东方在线美本助教号
回复【美本资料】获取
SAT阅读+文法+数学专项题型练习册
发布时间:2024-05-31添加新东方在线美本助教号
回复【美本资料】获取
机考SAT-可汗练习题
发布时间:2024-02-29添加新东方在线美本助教号
回复【美本资料】获取
机考SAT-CB官方样题
发布时间:2024-02-29添加新东方在线美本助教号
回复【美本资料】获取
《学科留学百问 (AP-IB-A Level)》
发布时间:2023-02-22添加新东方在线美本助教号
回复【美本资料】获取
2024中国学生留学备考白皮书
发布时间:2023-02-22添加新东方在线美本助教号
回复【美本资料】获取
2023北美考试一本通高中篇
发布时间:2023-02-22添加新东方在线美本助教号
回复【美本资料】获取
新东方SAT阅读讲义
发布时间:2023-02-06添加新东方在线美本助教号
回复【美本资料】获取
2023北美考试一本通高中篇
发布时间:2024-02-29关注美本留学家长帮微信订阅号
回复【美本资料】获取
2024中国学生留学备考白皮书
发布时间:2019-12-19添加新东方在线美本助教号
回复【美本】获取
《学科留学百问 (AP-IB-A Level)》
发布时间:2019-12-19添加新东方在线美本助教号
回复【美本资料】获取
机考SAT-CB官方样题
发布时间:2019-12-19添加新东方在线美本助教号
回复【美本资料】获取
机考SAT-可汗练习题
发布时间:2019-12-19添加新东方在线美本助教号
回复【美本资料】获取
SAT阅读+文法+数学专项题型练习册
发布时间:2019-11-28添加新东方在线美本助教号
回复【美本资料】获取

添加美本助教
即可获取美本资料大礼包

 推荐阅读
推荐阅读
在2024年的QS学科排名中,英国大学再次展现了他们在教育领域的卓越表现。这次排名中,英国大学在16个学科领域取得了世界第一的成绩,为其在全球教育界树立了新的标杆。
来源 : 网络整理 2024-04-23 11:16:49 关键字 : QS学科排名,英国大学qs学科排名
市场营销作为当代商业领域中至关重要的学科之一,一直备受关注。为了帮助读者更好地了解2024年全球市场营销学科的最新发展和排名情况,本文将介绍QS世界大学市场营销学科的排名榜单,并提供相关的官网链接供读者参考。
来源 : 网络整理 2024-04-23 10:21:37 关键字 : 市场营销学科排名,qs学科排名
备受关注的2024年酒店管理学科全球大学排名榜单终于揭晓,给全球学子带来了巨大的惊喜和期待。作为酒店管理学科领域的权威排行榜,该榜单汇集了各大知名院校和学者的投票和研究结果,为学生们提供了一份权威的选校参考指南。
来源 : 网络整理 2024-04-23 10:15:16 关键字 : 酒店管理学科排名,qs学科排名
每年QS世界大学统计与运筹学学科排名榜单都受到广泛关注,2024年的排名榜单也引起了极大的关注和讨论。首先,让我们来看一下2024QS世界大学统计与运筹学学科排名榜单的前几名。
来源 : 网络整理 2024-04-23 10:10:12 关键字 : 统计与运筹学学科排名,qs学科排名
随着2024QS世界大学经济与计量经济学学科排名榜单的发布,我们可以全面了解到这一领域的最新动态。本文将为您详细介绍2024QS世界大学经济与计量经济学学科排名榜单,解读其中的重点内容,并对我国相关大学在排名中的表现进行分析。
来源 : 网络整理 2024-04-23 10:03:55 关键字 : 经济与计量经济学学科排名,qs学科排名
最新发布的2024QS世界大学社会政策与行政管理排名榜单已经震动了全球教育界。这一排名榜单是依据世界知名教育机构QS(Quacquarelli Symonds)的权威数据和专业评估,为我们提供了一份准确且独具参考价值的全球大学排名。
来源 : 网络整理 2024-04-22 17:01:59 关键字 : 社会政策与行政管理学科排名,qs学科排名
社会学作为一门独具特色的学科,对于了解人类社会的发展和变迁起着举足轻重的作用。每年,QS世界大学社会学排名榜单会揭晓全球各大高等院校在这一领域的表现,并成为了各界人士瞩目的焦点。今天,让我们一起来揭晓2024年的榜单,并深入探讨排名的背后故事。
来源 : 网络整理 2024-04-22 16:56:00 关键字 : 社会学学科排名,qs学科排名
在当今竞争激烈的社会中,选择一所优秀的大学对我们的未来发展至关重要。随着法律行业的日益发展和全球化的趋势,了解和掌握国际上优秀的法律学府成为了无比重要的事情。而2024QS世界大学法律与法律研究排名榜单正是我们选择合适学府的权威指南。
来源 : 网络整理 2024-04-22 16:51:49 关键字 : 法律与法律研究学科排名,qs学科排名
2024QS世界大学教育与培训排名榜单,作为权威的评估之一,给出了全球范围内的学府排名。本次榜单覆盖了各个学科领域,综合评估了学校的教学质量、师资水平、科研实力等多个方面,旨在为学生和家长提供一个参考。
来源 : 网络整理 2024-04-22 16:48:08 关键字 : 教育与培训学科排名,qs学科排名
政治学作为一门研究人类政治行为、政治制度、政治思想等内容的学科,一直备受关注。近日,2024QS世界大学排名公布了最新的政治学学科排名榜单,引起了广泛的关注和讨论。
来源 : 网络整理 2024-04-22 16:38:53 关键字 : 政治学学科排名,qs学科排名

自动领取备考资料大礼包

1. 打开手机微信【扫一扫】,识别上方二维码;
2.添加【美本助教】,自动领取留学备考资料大礼包。

 SAT直播/精讲课
SAT直播/精讲课
 托福精讲系统课(旗舰版)
托福精讲系统课(旗舰版)
 托福直播VIP小班
托福直播VIP小班
 公开讲座
公开讲座
真实了解自己的水平,为备考做好规划!
价格 : ¥0元
真实了解自己的水平,为备考做好规划!
价格 : ¥0元
真实了解自己的水平,为备考做好规划!
价格 : ¥0元

 资料下载
资料下载
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
关注美本留学家长帮微信订阅号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取
添加新东方在线美本助教号
回复【美本资料】获取

自动领取备考资料大礼包

1. 打开手机微信【扫一扫】,识别上方二维码;
2.添加【Ella助教】,自动领取留学备考资料大礼包。
 阅读排行榜
阅读排行榜
 相关内容
相关内容